Differenzierungsbereich (Wahlpflichtbereich)
Unterrichtsinhalte (Beispiel)
Leistungsbewertung (mit Beispielen zu schriftlichen Arbeiten)
Der vorgestellte dreistündige Kurs stellt eine Kombination der Fächer Chemie und Physik dar. Die Wahl der Gegenstände begründet sich darin, dass hier Bereiche behandelt werden, die im Fachunterricht (erstes bzw. zweites und drittes Jahr) nur knapp angesprochen werden, Ergänzungen darstellen und fächerübegreifenden bzw. fächerverbindenden Charakter haben. Die Reihenfolge ist nicht als zwingend zu verstehen. Eine Umstellung ist dann notwendig, wenn auf Grundlagen der Fächer, die im Klassenverband unterrichtet werden, zurückgegriffen werden muss.
1. Untersuchung und Trennung von Stoffen:
2. Grundgesetze und deren Anwendung:
3. Der Einsatz des Computers:
Hier können z.B. die integrierten Programmpakete WORKS oder OFFICE zum Einsatz kommen.
Die Behandlung dieses Themas sollte nicht als Block, sondern an verschiedenen Stellen im
Kurs erfolgen.
4. Energiegewinnung und Energieverwertung:
5. Werkstoffe:
6. Umweltbereich Wasser:
7. Photographie und reprographische Methoden:
(zurück)
Kursarbeiten:
Im Differenzierungsbereich können pro Halbjahr zwei ein- bis zweistündige Kursarbeiten geschrieben werden. In der Regel dürften diese Arbeiten aus schulorganisatorischen Gründen einstündig sein. Statt der 2. Kursarbeit im Halbjahr kann eine andere Form der schriftlichen Leistungsüberprüfung gewählt werden (z.B. Facharbeit, Dokumentation).
Anforderungsbereiche der Kursarbeiten:
Im Unterricht behandelte Sachverhalte, Arbeitstechniken und Verfahrensweisen sollten in
angemessener Form wiedergegeben werden können.
Aus dem Unterricht bekannte Sachverhalte, Arbeitstechniken und Verfahrensweisen sollten
auf
ähnliche und vergleichbare Fragestellungen angewendet werden können.
Beispiele:
Ein bereits durchgeführter Versuch soll beschrieben und die bekannten Ergebnisse sollen
erläutert werden.
Eine fachspezifische Vorgabe (z.B. Messreihe) soll nach einer den Schülern bekannten
Methode ausgewertet werden.
>>> Beispiele
Andere Formen der schriftlichen Leistungsüberprüfung als Ersatz einer Kursarbeit:
Hier kann z.B. ein im Unterricht über mehrere Stunden behandeltes Thema noch einmal unter
ganz bestimmen Fragestellungen zusammenhängend dargelegt werden.
Es kann auch ein im Unterricht nur knapp eingeführtes Thema selbstständig auf Grundlage
vorgegebener oder selbst zu beschaffender Materialien und eingeübter Arbeitstechniken
erarbeitet werden, vergleichbar einem Referat.
Es könnte auch eine ausführliche Dokumentation eines Themas über eine Internetrecherche
erstellt werden.
Bei allen Formen solcher Leistungsüberprüfungen muss aber der individuelle Charakter
deutlich werden.
Bewertet wird bei den schriftlichen Leistungsüberprüfungen nicht nur die sachliche Richtigkeit sondern auch das Darstellungsvermögen unter Berücksichtigung der allgemeinsprachlichen Richtigkeit.
Sonstige Mitarbeit:
Hier gelten die allgemeinen Kriterien der Leistungsbewertung.
(zurück)
Aufgabenbeispiele zu schriftlichen Kursarbeiten
1. Beispiel:
Eine Mischung aus Wasser und Alkohol soll weitgehend in die reinen Stoffe getrennt werden.
1. Fertige eine beschriftete Skizze der Versuchsapparatur an.
2. Beschreibe die Versuchsdurchführung.
3. Erkläre, aufgrund welcher Stoffeigenschaften die Trennung funktioniert.
4. Lege dar, ob eine vollständige Trennung des Gemischs möglich ist.
4. Wie könnte man in Abänderung der verwendeten Versuchsapparatur
den Siedepunkt des reinen Alkohols bestimmen?
2. Beispiel:
Gegeben ist folgende Messreihe, die beim Erwärmen von Fixiersalz aufgenommen wurde:
| Minuten | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| oC | 20 | 25 | 31 | 35 | 41 | 45 | 48 | 48 | 48 | 53 | 59 |
1. Trage die Temperatur in Abhängigkeit von der Zeit grafisch auf und
beschreibe den erhaltenen Graphen.
2. Gebe begründet an, welchen Schmelzpunkt Fixiersalz hat.
3. Gebe im erstellten Diagramm an, wo der feste und flüssige Aggregatzustand
vorliegen.
4. Beschreibe die Versuchsdurchführung mit Versuchsskizze, die zu der gegebenen
Messreihe führt.
5. Die Löslichkeit von Fixiersalz beträgt bei 20 oC 70 g in 100 g
Wasser.
Wie kann man die Löslichkeit experimentell bestimmen?
Wie viel g Fixiersalz und Wasser sind in 750 g einer Lösung mit einem
Massenanteil von 10 %?
3. Beispiel:
Ein wasserunlösliches Farbstoffgemisch aus drei Farbstoffen (rot, gelb,
grün) soll mit Hilfe der Dünnschichtchromatographie getrennt werden. Als
Laufmittel wird ein Gemisch aus Benzin und Toluol verwendet.
Die Rf-Werte betragen:
Rf1 = 0,5 (roter Farbstoff)
Rf2 = 0,3 (gelber Farbstoff)
Rf3 = 0,8 (grüner Farbstoff)
4. Beispiel:
Es sollen 30 g Eisensulfid (FeS) aus den Elementen hergestellt werden.
Atommassen: m(Fe) = 55,9 u m(S) = 32,1 u
Lösung zu 2.: m(Fe) = 19,05 g m(S) = 10,95 g
5. Beispiel:
In Anlage befinden sich europäische Wetterkarten vom 20. und 21.04.1999.
1. Beschreibe für beide Tage die Lage von Tief- und Hochdruckgebieten.
Wie haben sich die Druckgebiete verlagert?
2. Beschreibe für beide Tage die Lage der Wetterfronten (Kalt-, Warmfronten,
Okklusionen) und gebe an, wie sich die Fronten verändert haben.
3. Ermittle für die Städte London, Paris, Köln und Rom für beide Tage Luftdruck,
Temperatur, Windstärken (m/s), Windrichtung Bedeckungsgrad und
Niederschläge.
4. Beschreibe den Verlauf der Isobare 1000 hPa für den zweiten Tag.
5. Gebe begründet an, wie sich das Wetter für den 22.04.1999 für den Ort Köln
in etwa verändern könnte.
6. Beispiel:
In einer Heizungsanlage (Ölbetrieb) mit einem Wirkungsgrad von 80 % sollen 300 L Wasser im Wärmespeicher von 20 auf 70 oC erwärmt werden.
Angaben:
Heizwert von Heizöl = 42700 kJ/Kg
Preis von Heizöl = 0,5 €/kg
spezifische Wärmekapazität von Wasser = 4,19 kJ/(kg*K)
Lösung zu 1.:
Wärmemenge: W = 75420 kJ Masse Heizöl: m =
1,77 kg Preis = 0,88 €
7. Beispiel:
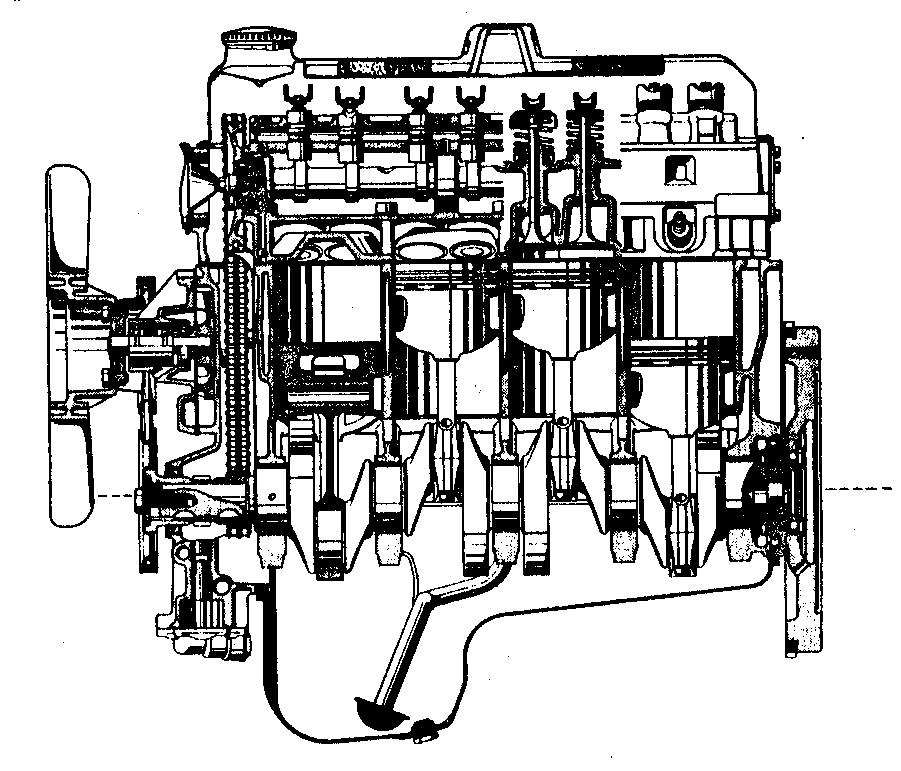
Aus der Abbildung ist der Aufbau eines Viertaktmotors zu sehen (Benzinmotor, Zündfolge 1-3-4-2).

1. Erkläre mit Skizze den durchgeführten Modellversuch zum Verbrennungsmotor.
2. Erkläre die grundsätzliche Funktionsweise eines Viertaktmotors und die
Kraftübertragung auf das Schwungrad.
3. Lege für den abgebildeten Motor dar, welche Arbeitstakte die anderen Zylinder
ausführen, wenn Zylinder 1 gezündet wird.
4. Erkläre mit den entsprechenden Fachbegriffen, wie bei dem abgebildeten Motor
die Ventilsteuerung funktioniert.
5. Für den Betrieb des Motors benötigt man Superbenzin mit einer Octanzahl >95 .
Was versteht man unter der Octanzahl und warum ist dieses Benzin
notwendig?
8. Beispiel:
Ein geothermisches Heizwerk fördert stündlich 200 m3 Wasser mit einer Temperatur von 80 oC aus 1000 m Tiefe nach dem Hot-Dry-Rock-Verfahren. Nach Übergabe an einen Wärmeaustauscher ist das Wasser auf 40 oC abgekühlt.
Angaben: c (Wasser) = 4,19 kJ/(kg*K) Heizwert (Heizöl) = 41000 kJ/kg
Lösung zu 2.: Leistung: P = 9,3
MW Energie: W = 2,9364 * 108 MJ
Lösung zu 3.: 2387 Haushalte
9. Beispiel:
50 g einer Bodenprobe werden mit verdünnter Salzsäure im Überschuss versetzt.
Man erhält ein Gasvolumen von 360 ml.
1. Welche chemische Reaktion läuft beim Versetzen mit Salzsäure ab?
Gebe hierzu auch die Reaktionsgleichung an.
2. Berechne den Massenanteil von Kalk in der Bodenprobe und begründe
alle Rechenschritte.
3. Beschreibe und erkläre mit allen Reaktionen den technischen Kreislauf
des Kalks und gebe an, welche Bedeutung Kalk als Baustoff hat.
Angaben:
m (Ca) = 40 u m (C) = 12 u m
(O) = 16 u Vm (Gas) = 24 L/mol (20 oC)
Lösung zu 2.: Massenanteil = 3 %
(zurück)
Extraktion von Pflanzenfett
Ein großes Reagenzglas wird etwa 4 cm hoch mit Kokosflocken
oder Kokosraspeln gefüllt. Diese Portion ist vorher genau abzuwiegen. In dem
Reagenzglas werden die Kokosflocken mit Leichtbenzin übergossen, wobei das
Benzin etwa 1 cm über den Flocken stehen soll. Das Reagenzglas wird in einem
Wasserbad (Temperatur ca. 60 oC) mehrere Minuten unter Schütteln
erwärmt.
Danach wird die Lösung abfiltriert. Das Filtrat wird auf eine Glasschale
gegossen, die zuvor gewogen wurde. Man lässt das Benzin im Freien verdunsten
und wiegt danach die Glasschale mit dem Rückstand.
Auswertung: Der Massenanteil von Fett in den Kokosflocken soll berechnet werden.
Frage: Wie könnte man den Versuch abändern, um die Ausbeute von Fett zu erhöhen und das Benzin wiederzugewinnen?
Sicherheitshinweise: Das Benzin ist leichtentzündlich. Daher sind offene Flammen und Zündquellen unbedingt zu vermeiden!
(zurück)
Trennung von Blattfarbstoffen
Gewinnung der Farbstofflösung:
Grüne Blätter, die man zuvor im Dunkeln leicht getrocknet hat, werden
zerkleinert und mit einer Spatelspitze Quarzsand und Calciumcarbonat in einem
Mörser zerrieben. Das Gemisch gibt man in einen Erlenmeyerkolben (100 mL). Nach
Zugabe von 30 mL Aceton wird der Kolben mit einem Stopfen verschlossen und der
Inhalt ca. 5 Minuten geschüttelt. Die Lösung wird abfiltriert und in einer
braunen Flasche aufbewahrt.
Trennung des Farbstoffgemischs:
Das Farbstoffgemisch wird mit Hilfe der Papierchromatographie und der
Dünnschichtchromatographie (DC) getrennt.
Ein Tropfen der Farbstofflösung wird mit einer Mikropipette jeweils auf der
Startlinie aufgetragen und leicht angetrocknet.
Laufmittel für die Papierchromatographie: Gemisch aus 10 mL Benzin, 2 mL Petrolether, 2 mL Aceton
Laufmittel für die Dünnschichtchromatographie: Gemisch aus 5 mL Benzin, 5 mL Petrolether, 1 mL 2-Propanol
Sicherheitshinweise: Die Lösungsmittel sind leichtentzündlich. Daher sind offene Flammen und Zündquellen unbedingt zu vermeiden!
(zurück)