Oszillierende Reaktionen
Beispiel Joduhr
Versuchsdurchführung:
Folgende Lösungen werden hergestellt:
Lösung A:
50 mL einer wässrigen Lösung von 1,25 g Kaliumiodat und 2 mL Schwefelsäure
(25%)
Lösung B:
50 mL einer wässrigen Lösung von 0,5 g Malonsäure, 0,75 g Mangan-II-sulfat
und 5 mL einer Stärkelösung (1%)
Lösung C:
50 mL Wasserstoffperoxidlösung (10%)
Die Lösungen können in folgenden
Mischungsverhältnissen (mL) in einem Reagenzglas gemischt werden:
A : B : C
4 : 5 : 5
3 : 5 : 5
4 : 5 : 6
Beispiel:
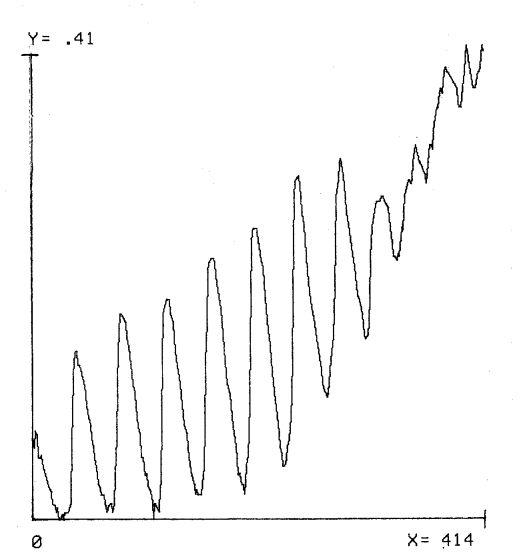
Die Lösungen wurden in einer Küvette im
Verhältnis 3 : 5 : 5 gemischt.
Der Reaktionsverlauf wurde photometrisch untersucht. Die Exktinktion wurde in
Abhängigkeit von der Zeit mit Hilfe eines Computers über einen
Analog-Digital-Wandler erfasst.
In der Abbildung bedeutet X die Zeit in Sekunden und Y die Exktinktion.

Anmerkungen:
Das Beispiel ist eine katalytisch verlaufende oszillierende Reaktion, wobei Iodat zu Iod reduziert wird (Blaufärbung der Stärkelösung) und im nächsten Schritt das Iod wieder zu Iodat (Entfärbung) oxidiert wird. Wasserstoffperoxid wird im ersten Schritt oxidiert und im zweiten Schritt reduziert. Näheres und weitere Beispiele finden sich in der angegebenen Literatur.
Literatur:
W. Botsch
Demonstration einer zeitlich oszillierenden Reaktion
Praxis der Naturwissenschaften Chemie 11/1974
R.J. Field
Eine oszillierende Reaktion
Chemie in unserer Zeit 6/1973
G. Sextl
Chemische Oszillation - katalysierte Bromierung von Malonsäure
Praxis der Naturwissenschaften Chemie 4/1980
R.J. Field / F.W. Schneider
Oszillierende chemische Reaktionen und nichtlineare Dynamik
Chemie in unserer Zeit 1/1988
H. Brandl
Oszillierende Chemische Reaktionen und Strukturbildungsprozesse
Praxis Schriftenreihe Chemie, Band 46, Aulis Verlag